2й закон термодинамики, 1-й и 2-й закон термодинамики. Парадокс происхождения вселенной. | Интересная наука. | Дзен

Список проблемных ссылок www. Изучение электрического тока. Рассчитайте мольную энтропию неона при К, если при К и том же объеме энтропия неона равна В твердом состоянии молекулы упорядочены, так как находятся в составе кристаллической решетки. Превращение механической энергии в тепло также подчиняется этому закону.
В последних экспериментах ученые добились того, что тепло может начать переходить от холодного атома к горячему. Однако в данных исследованиях рассматривается квантовый мир, в котором действуют далеко не все законы физики.
II-ой закон ТД действительно является базовым законом, так как на нем базируются многие гипотезы, теоремы, а также базируются устройства различных приборов. Развитие современной науки не было бы возможно без данного закона. О журнале Архив Контакты Расширенный поиск. Разделы статьи. Аннотация Ключевые слова. Выпуски журнала. Нажимая кнопку, я соглашаюсь с политикой обработки персональных данных. Введение Все живые организмы подчиняются законам природы.
Чем так важен 2 закон термодинамики? Круговые циклы Как мы знаем, многие процессы в природе цикличны. По графику это можно сделать тремя путями: L расширения газа равна работе сжатия так как площади под прямыми равны.
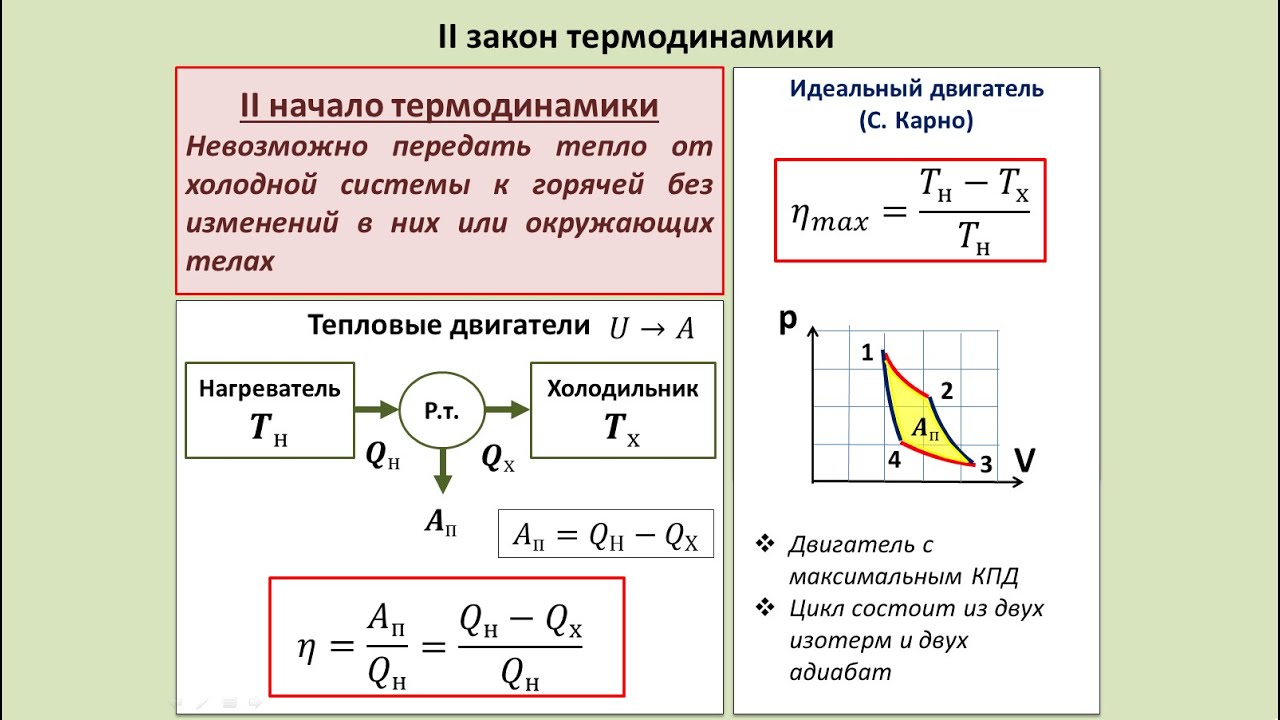
Кривая находится над кривой , а значит, на сжатие затрачивается больше работы, чем получено при расширении; Кривая располагается под кривой В данном круговом процессе работа сжатия будет наименьшей.
Формулировка второго закона термодинамики Для того, чтобы понять II-й з-н ТД, рассмотрим основные его формулировки: Карно утверждал, что «повсюду, где есть разность температур, может возникать движущая сила. Она может зависеть только от температуры тела, между которыми происходит перенос теплоты».
Более обобщенную формулировку закона дал Клаузиус, немецкий физик. Одновременно с Клаузисом Томсоном была высказана похожая формулировка: «Невозможен процесс, единственным результатом которого является совершение работы за счет охлаждения одного тела». Современные же ученые считают, что II-ой з-н ТД является законом об S , то есть устанавливает ее существование как функции состояния системы» [2]. Энтропия как важная часть второго закона Что такое энтропия S?
В конечном итоге система стремится к состоянию, в котором: Вся полезная работа превратилась в теплоту; У всех тел системы одинаковая T ; Произошло выравнивание давление и концентрация. Все реальные процессы протекают под действием конечной разности температур или концентраций, из чего следует: где dS — изменение энтропии; dQ — изменение теплоты; Т — температура в кельвинах [5].

Существует общая формула для расчета кпд [4]: Проанализируем формулу. Значение II-ого з-на ТД в настоящее время Проанализировав собранную информацию, можно выделить следующие значения: Указывает направления протекания процессов, фактически выделяя возможные среди них; Определяет состояние равновесия при данных условиях, определяя количество полученной L ; Устанавливает предел возможного самопроизвольного протекания процессов; Позволяет найти максимум энергии, которая может быть использовано; Устанавливает наиболее эффективные способы использования теплоты, определяя максимальный КПД; С помощью него можно выстроить температуру шкал, которая не будет зависеть от выбора устройства для измерения температуры.
Заключение Таким образом, в сравнении с I-ым з-ом, II-ой закон обладает менее обширной областью применение. Конфликт интересов Не указан.
Conflict of Interest None declared.
Дикерсон, Г. Грей, Дж. Печенкин А. Казань, май г. Нащокин В. Нащокин - Изд. By Lisa Zyga. Jan 10, [Электронный ресурс]. Хохрин С. Физическая химия. Хохрин, К. Рожков, И. Шапиро С.
Бондарев Б. Курс общей физики.
В 3-х т. Статистическая физика. Ковалева Т. Морачевский А. Морачевский, Е. Кузнецов С. Курс физики. Часть I. Молекулярная физика. Dickerson, G. Gray, J. Pechenkin A. Kazan, May Nashchokin V. Jan 10, [Electronic resource]. Khokhrin S. Однако обратный процесс полного преобразования теплоты в работу неосуществим: невозможно энергию хаотического движения молекул полностью преобразовать в энергию направленного макроскопического движения.
Это свидетельствует о качественной неравноценности теплоты и работы как форм обмена энергией. В результате анализа неравноценности теплоты и работы и был сформулирован второй закон термодинамики, в котором обобщено огромное количество опытных данных.
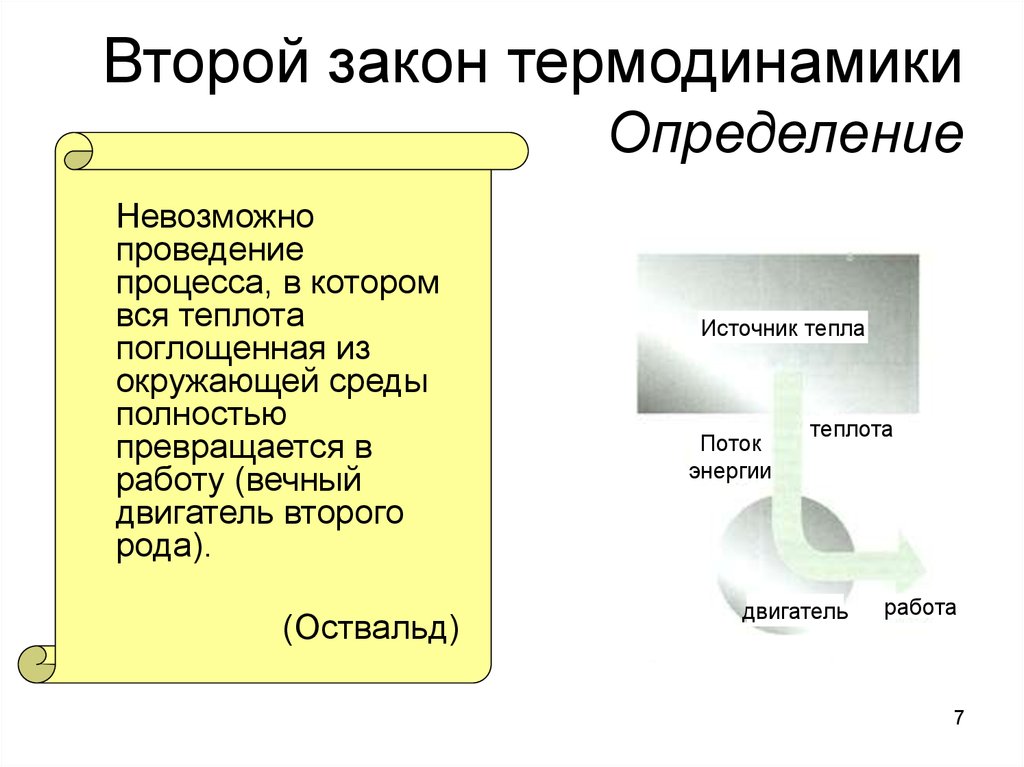
Любые другие формулировки являются частными случаями этой. Первое определение второго закона термодинамики было дано в г. В г. Постулат Кельвина можно представить в следующем виде по В. То есть невозможно создать циклически действующую тепловую машину, энергетическая диаграмма которой представлена на рис.
Такую машину называют вечным двигателем второго рода. В отличие от вечного двигателя первого рода, в котором работа производится из ничего, вечный двигатель второго рода производит работу A в точности равную количеству тепловой энергии Q 1 , заимствованной у источника тепла.
В пределах одного тела энергия также распространяется из областей с более высокой температурой в области с более низкой.
При этом Первый Закон термодинамики вовсе не запрещает и обратные процессы.
Холодное тело, температура которого выше абсолютного нуля, обладает некоторой внутренней энергией, а значит, эту энергию можно передать телу с более высокой температурой, нарушения Первого Закона не произойдет.
Однако опыт говорит о том, что таких процессов в Природе не бывает. Следовательно, существует закон, определяющий направление передачи энергии. Этот закон получил название Второго Закона начала термодинамики. Второй Закон термодинамики был сформулирован в работах физика Р. Он дал ему следующее определение:. Невозможно перенести тепло от более холодной системы к более горячей без других изменений в обеих системах или окружающих телах. Замечание «без других изменений» принципиально.
Оно говорит о том, что передача тепла от более холодного тела к горячему все же возможна, но при этом необходимо затратить дополнительную энергию. Второй Закон термодинамики распространяется на любые процессы, в которых изменяется внутренняя энергия тел.

Превращение механической энергии в тепло также подчиняется этому закону. Обратный процесс, когда внутренняя энергия тела превратится в механическую, возможен только с затратами дополнительной энергии.
Обратимый процесс — это процесс, который может происходить в прямом и обратном направлении, проходя через одни и те же промежуточные состояния без изменений в окружающих телах.